Déterminants moléculaires du remodelage cardiaque et de l’insuffisance cardiaque
Équipe 2 – UMR1167 – Inserm – Université de Lille – CHU Lille – Institut Pasteur de Lille
Présentation
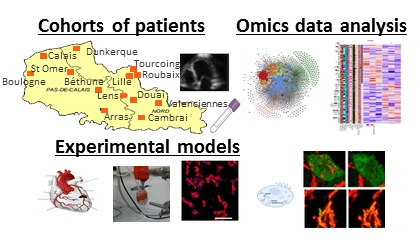
L’équipe “Déterminants moléculaires du remodelage et de l’insuffisance cardiaque” est composée de chercheurs, de chercheurs hospitalo-universitaires cliniciens, de chercheurs post-doctorants, d’ingénieurs, de techniciens et d’étudiants. Elle développe une recherche translationnelle du lit du malade à la paillasse. Elle met en oeuvre et utilise des techniques avancées de médecine expérimentale (modèles cellulaires et animaux), de protéomique et de bioinformatique.
Objectifs de l’équipe : Trouver de nouveaux biomarqueurs pour le diagnostic et le pronostic du remodelage cardiaque après un infarctus du myocarde et une insuffisance cardiaque et caractériser les mécanismes physiopathologiques en développant une recherche translationnelle en interface entre l’hôpital cardiologique et le laboratoire.
(1) Identifier des biomarqueurs circulants du remodelage cardiaque et de l’insuffisance cardiaque par de nouvelles approches de criblages systématiques ;
(2) Valider cliniquement les biomarqueurs identifiés ;
(3) Identifier et décrypter les mécanismes physiopathologiques des cibles identifiées comme impliquées dans l’insuffisance cardiaque.
Actus
- Dotation Fédération Française de Cardiologie.
Prédiction du remodelage cardiaque par une approche de protéomique à haut débit (CHU de Lille, Inserm, Univ Lille, Inria) (2020-2021).
L’objectif de ce projet est d’utiliser une technique de protéomique à haut débit permettant de doser plus de 5000 protéines dans un simple échantillon de plasma (technique SOMASCAN) pour prédire le remodelage après infarctus. Les dosages ont été réalisés dans les échantillons plasmatiques des patients inclus dans les études REVE et REVE-2. Les perspectives en termes de recherche et de santé publique sont une meilleure stratification du risque d’insuffisance cardiaque après un infarctus et aussi une meilleure connaissance physiopathologique qui pourrait permettre de nouvelles recherches thérapeutiques.
- Dotation Fédération Française de Cardiologie (Paris, Créteil, Lille).
Rôle de la protéine PrPc dans la physiopathologie du remodelage ventriculaire gauche après l’infarctus du myocarde (2021-2022).
Les objectifs de ce projet sont 1) de préciser le rôle de PrPc dans le remodelage ventriculaire gauche post-infarctus, 2) évaluer le potentiel de PrPc comme cible thérapeutique, 3) affiner la valeur prédictive des taux sanguins de PrPc dans la prédiction du remodelage ventriculaire gauche et la survenue d’éléments cliniques.
- FHU-CARNAVAL: CArdiac Research Network on Aortic Valve and heart failure (Caen-Rouen-Amiens-Lille (2021-2025).
Le projet CARNAVAL a pour objectif 1) de mieux comprendre la physiopathologie de l’insuffisance cardiaque et du rétrécissement aortique, 2) d’identifier de nouvelles cibles thérapeutiques basées sur les résultats précliniques, 3) d’évaluer de nouvelles méthodes d’analyse des données, 4) de proposer de nouvelles méthodes de prise en charge, 5) d’aborder la question du parcours de soin d’un patient traité TAVI, 6) de formuler et répondre à des questions éthiques autour des techniques innovantes, 7) de proposer de nouvelles formations originales et de mener des actions de sensibilisation grand public.
Projets transversaux
 Collaboration avec les équipes du CIIL (M. Pichavant, I. Wolowczuk, C. Grangette, P. Brodin : CONNECTING et COMMONLY.
Collaboration avec les équipes du CIIL (M. Pichavant, I. Wolowczuk, C. Grangette, P. Brodin : CONNECTING et COMMONLY.
Ces projets sont développés dans le cadre du CPER Longévité.
Le projet CONNECTING (2017-2018) vise à comprendre comment l’association « consommation d’un régime riche en gras et exposition chronique à la fumée de cigarette » peut avoir des effets délétères sur les compartiments cardiovasculaire, pulmonaire, métabolique et intestinal. Ce projet a pour objectif de comprendre les mécanismes cellulaires et moléculaires impliqués dans les effets délétères observés.
Le projet COMMONLY (2019-2020) vise à approfondir le rôle du stress oxydant dans les effets délétères du régime riche en lipides associé à la fumée de cigarettes. Le rôle du gène immuno-sensible 1 (IRG1) – un facteur impliqué dans la modulation des espèces réactives de l’oxygène et la production d’acide itaconique – dans les effets néfastes pour la santé de la co-exposition à la cigarette et à un régime riche en gras sera étudié, au niveau de l’organisme entier et des tissus (poumons, tissus adipeux, cœur et intestin).
 Collaboration avec l’équipe d’Eric Boulanger qui nous a permis d’avoir un projet financé (RAGING) 2018-2020 (IPL – UdL – HEI).
Collaboration avec l’équipe d’Eric Boulanger qui nous a permis d’avoir un projet financé (RAGING) 2018-2020 (IPL – UdL – HEI).
L’inflammaging, contraction des termes “inflammation” et “aging”, correspond à un état d’inflammation de bas grade, diffus dans l’organisme, évoluant à bas bruit, sans foyer inflammatoire manifeste. Cette inflammation systémique constitue le substrat commun à la plupart des maladies chroniques liées au vieillissement (maladies d’Alzheimer, Parkinson, athérosclérose, maladies cardiovasculaires, DMLA, diabète de type II, ostéoporose, cancer…) L’inflammaging augmente non seulement la morbidité et la mortalité, mais impacte également fortement la qualité de vie des patients. Par conséquence, l’identification des processus biologiques permettant de le maîtriser est essentielle pour permettre à la population de « mieux vieillir ». Les objectifs du projet sont de concevoir, sélectionner, développer et tester (in vitro/in vivo) des antagonistes de RAGE pour évaluer le rôle global de RAGE dans l’inflammaging. Le projet est divisé en 2 taches principales :
- Développer des antagonistes de RAGE
- Evaluer biologiquement les antagonistes développés
Membres
Florence PINET
DR1 Inserm, responsable d’équipe
Numéro ORCID : 0000-0002-5471-1487
Christophe BAUTERS
PU-PH Univ Lille/ CHU Lille
Numéro ORCID : 0000-0001-8268-8467
Pascal DEGROOTE
PH CHU de Lille
Numéro ORCID : 0000-0002-6211-0147
Nicolas LAMBLIN
PU-PH Univ Lille/ CHU Lille
Numéro ORCID : 0000-0003-3754-1241
Olivia BESEME
Ingénieur d’étude, Univ Lille
Maggy CHWASTYNIAK
Technicienne IPL
Émilie DUBOIS-DERUY
Post-doc
Annie TURKIEH
Post-doc
Fadi ABOU ZEID
Étudiant en thèse
Wilfried HEYSE
Étudiant en thèse
Victoriane PEUGNET
Étudiant en thèse
Yara EL MASRI
Étudiant en Master
Fréderic NAVEZ
Étudiant en Master
Julian LALOYAUX
Étudiant en Licence
Fabien DWORNIKOWSKI
Étudiant en Licence
Guillaume MACHADO
Étudiant en Licence
Publications
Gupta SK, Foinquinos A, Thum S, Remke J, Zimmer K, Bauters C, de Groote P, Boon R, de Windt L, Preissl S, Hein L, Batkai S, Pinet F, Thum T (2016).
Preclinical development of a microRNA-based therapy for the infarcted heart of elderly individuals.
J Am Coll Cardiol 66:1557-71. doi: 10.1016/j.jacc.2016.07.739.
Turkieh A, Fertin M, Bouvet M, Mulder P, Drobecq H, Lemesle G, Lamblin N, de Groote P, Porouchani S, Chwastyniak M, Beseme O, Amouyel P, Mouquet F, Balligand JL, Richard V, Bauters C, Pinet F (2018).
Expression and implication of clusterin in left ventricular remodeling after myocardial infarction.
Circ- Heart Fail. 11(6):e004838. doi: 10.1161/CIRCHEARTFAILURE.117.004838.
Turkieh A, Porouchani S, Beseme O, Chwastyniak M, Amouyel P, Lamblin N, Balligand JL, Bauters C, Pinet F (2019).
Increased clusterin levels after myocardial infarction protects cardiomyocytes from apoptosis induced by a defect in protein degradation systems activity.
Cell Death Dis. 10(8):608. doi: 10.1038/s41419-019-1857-x.
Cuvellier M, Vandewalle V, Brunin M, Beseme O, Hulot A, de Groote P, Amouyel P, Bauters C, Marot G, Pinet F. (2019).
Circulating proteomic signature of early death in heart failure patients with reduced ejection fraction.
Sci Rep Dec 16;9(1):19202. doi: 10.1038/s41598-019-55727-1.
Perdomo L, Vergori L, Duluc L, Vidal-Gomez X, Soleti R, Chwastyniak M, Bisserier M, Le Lay S, Villard A, Simard G, Meilhac O, Lezoualc’h F, Khantalin I, Veerapen R, Dubois S, Boursier J, Henni S, Gagnadoux F, Pinet F, Andriantsitohaina R, Martinez MC. (2020).
Microvesicles-associated RAP1 accumulates in atherosclerotic plaques, correlates with vascular risks and mediates early steps of atherosclerosis.
Circ Res Aug 28;127(6):747-760. doi: 10.1161/CIRCRESAHA.120.317086.
Mots-clés
Insuffisance cardiaque ; Stress oxydant ; Biomarqueurs ; Protéomique